Studiare la sicurezza dei farmaci in gravidanza: Il contributo del progetto PROTECT
La sicurezza dei farmaci in gravidanza resta una delle aree più complesse e meno esplorate della medicina. Le donne incinte sono generalmente escluse dagli studi clinici e i modelli animali non sempre riescono a prevedere con precisione gli effetti dei farmaci sul feto umano.
Per colmare questo vuoto nasce PROTECT, progetto vincitore di un ERC Proof of Concept, guidato dal Professor Alessandro Filippo Maria Pellegata all’interno del LaBS-3D Bioprinting and Tissue Engineering.
Perché la sicurezza dei farmaci in gravidanza è ancora oggi un ambito con così tante incertezze scientifiche?
Il motivo principale è che, in gravidanza, si applica un principio di massima cautela: se non si conoscono con certezza gli effetti di qualcosa, nel dubbio si evita di utilizzarla. Questo perché è estremamente difficile condurre studi diretti sulla tossicità fetale dei farmaci. Di conseguenza, per molti farmaci non si sa con precisione quale sia l’effetto sul feto durante la gravidanza e, per non correre rischi, si preferisce non somministrarli.
Nella storia ci sono stati casi eclatanti di farmaci ritenuti inizialmente sicuri che si sono poi rivelati dannosi per il feto. Anche per questo motivo, oggi si adotta un approccio particolarmente prudente.
Esistono numerosi studi sulla tossicità nelle fasi iniziali della gravidanza, in particolare durante lo sviluppo embrionale. Sono invece molto più limitati i dati relativi alle fasi successive, come il secondo e il terzo trimestre.
E perché ci sono più studi sulla fase embrionale rispetto a quella più avanzata?
In parte perché esiste già una vasta letteratura scientifica sulla fase embrionale. Questo interesse non nasce originariamente dallo studio della tossicità fetale dei farmaci, ma piuttosto dalla biologia dello sviluppo: l’obiettivo era comprendere i meccanismi e i processi che avvengono nelle prime fasi della vita. Questo ha portato alla disponibilità di numerosi modelli sperimentali per studiare lo sviluppo embrionale.

Coltura di cellule da fluido amniotico condotta in cappa biologica - Credits: Valerio Fausti
All’interno del vostro progetto di ricerca, vi state focalizzando su trimestri o fasi specifiche della gravidanza?
Sì. Le cellule che riusciamo a ottenere provengono da gravidanze di almeno 17 settimane di età gestazionale. Questo significa che lavoriamo principalmente sul secondo e terzo trimestre. Prima sarebbe infatti molto più complicato, almeno non con procedure minimamente invasive e sicure. Qualsiasi prelievo deve infatti avvenire senza introdurre rischi aggiuntivi per la madre. Questo vincolo limita inevitabilmente il periodo su cui possiamo lavorare.
Quali sono i principali rischi per le donne incinte quando devono assumere farmaci?
I rischi si collocano su due livelli distinti ma interconnessi: quello materno e quello fetale.
Da un lato, c’è il rischio che un farmaco possa avere effetti tossici sul feto, interferendo con il suo sviluppo. Dall’altro, però, la mancata somministrazione di un farmaco può rappresentare un problema per la salute della madre, soprattutto in presenza di patologie croniche o progressive.
Un esempio emblematico riguarda alcune malattie neurodegenerative, che richiedono terapie continuative per rallentare la progressione dei sintomi. In questi casi, interrompere il trattamento può avere conseguenze significative. Ci sono situazioni in cui una donna, nel momento in cui decide di avere un figlio, deve sospendere la terapia per un periodo molto lungo: non solo durante la gravidanza, ma anche nei mesi precedenti al concepimento — per consentire l’eliminazione del farmaco dall’organismo — e durante l’allattamento. Questo può tradursi in una sospensione complessiva della terapia anche di due o tre anni, con potenziali ripercussioni sulla salute materna.
Accanto a questi aspetti più critici, esiste anche una dimensione legata alla qualità della vita. Alcuni farmaci, non necessariamente salvavita o legati a terapie croniche, che migliorano il benessere quotidiano, non vengono utilizzati in gravidanza per l’incertezza sui loro effetti.

Alessandro Filippo Maria Pellegata
Qual è il tuo percorso accademico-professionale? Che cosa ti ha portato a interessarti di questo ambito?
Il mio percorso accademico si è svolto principalmente al Politecnico di Milano, dove mi sono laureato in Ingegneria Biomedica e ho poi conseguito un dottorato in Bioingegneria. Durante il dottorato ho iniziato a lavorare nel campo della medicina rigenerativa, occupandomi dello sviluppo di soluzioni ingegnerizzate, basate su tecniche biotecnologiche, per la ricostruzione di organi e tessuti.
Successivamente mi sono trasferito a Londra, dove ho lavorato per diversi anni come ricercatore postdoc presso UCL. Anche lì mi sono occupato di medicina rigenerativa, un ambito in cui continuo a lavorare tuttora, con un focus particolare sul contesto pediatrico: sia su patologie congenite, quindi diagnosticabili anche in fase prenatale, sia più in generale su condizioni legate al periodo prenatale e neonatale.
Com’è nata l’idea del progetto PROTECT?
L’idea nasce dalla convergenza di diversi elementi. Da un lato, negli ultimi anni di ricerca ho sviluppato una forte competenza nello studio delle cellule del fluido amniotico. Dall’altro, hanno avuto un peso anche mie esperienze interpersonali, legate a persone che si sono trovate ad affrontare difficoltà nella gestione di terapie farmacologiche durante la gravidanza. A questo si aggiunge l’esperienza maturata nel campo della modellistica in vitro.
Mettendo insieme questi tre aspetti — competenze tecniche, esperienza nella ricerca e consapevolezza del problema clinico — è nata l’idea del progetto: sviluppare uno strumento che possa contribuire ad aumentare le conoscenze sugli effetti dei farmaci sul feto durante la gravidanza.
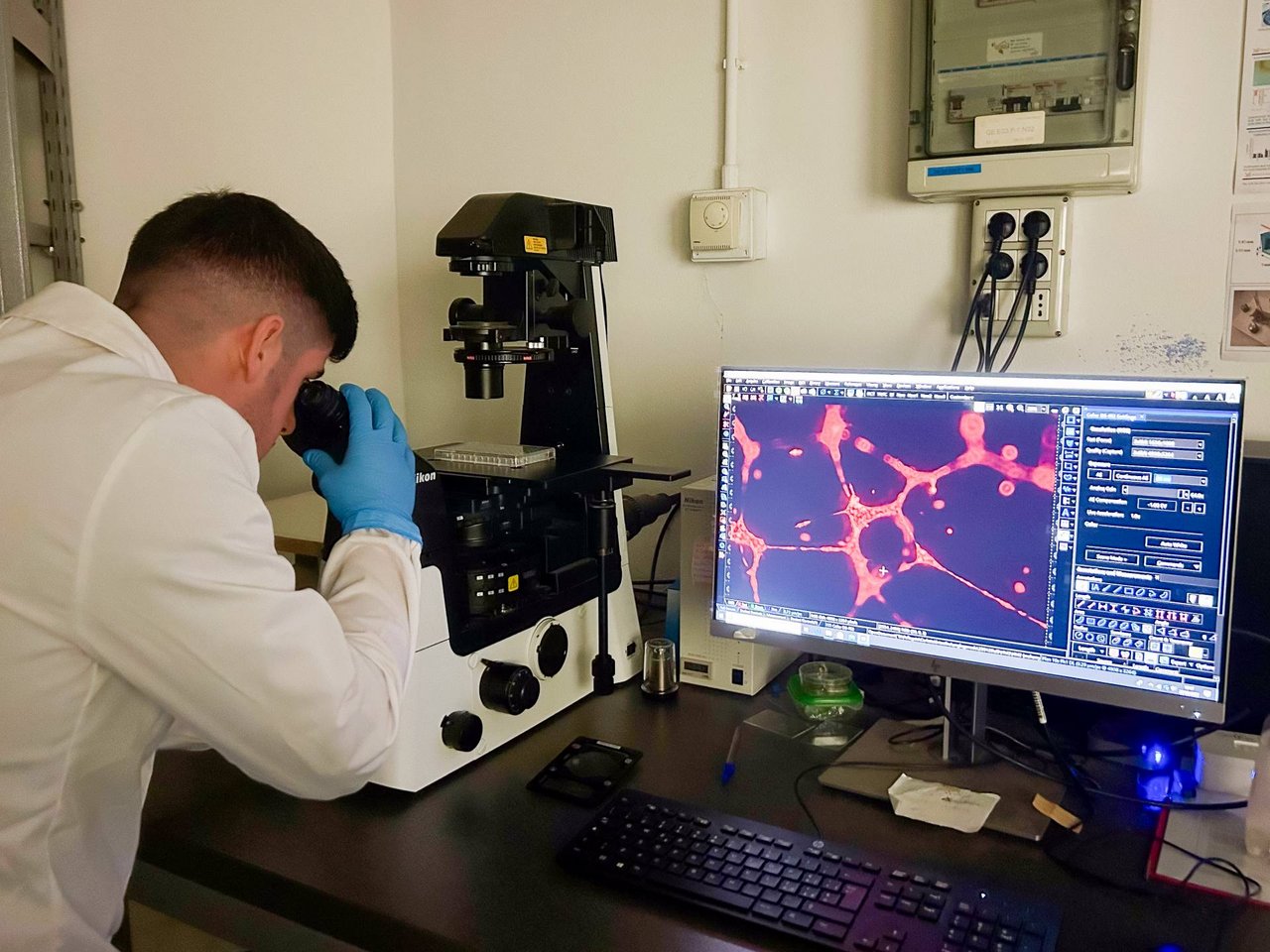
Osservazione al microscopio a fluorescenza di strutture vascolari in-vitro - Credits: Valerio Fausti
Quali sono le varie fasi del progetto e in quale fase vi trovate in questo momento?
L’obiettivo del progetto è sviluppare una piattaforma sperimentale in cui cellule provenienti dal fluido amniotico vengono organizzate in strutture tridimensionali tramite tecniche di bioprinting. In pratica, si tratta di “stampare” piccoli costrutti tridimensionali contenenti queste cellule, in modo standardizzato, replicabile e riproducibile su larga scala.
Una volta realizzato questo sistema, il passo successivo sarà la validazione del modello. Prima di poter generare nuova conoscenza, infatti, è fondamentale dimostrare che il modello è affidabile e in grado di riprodurre risultati già noti. Per questo motivo, in questa prima fase — che coincide con la durata del progetto, pari a 18 mesi — testeremo farmaci di cui è già conosciuto il profilo di sicurezza o di tossicità fetale, sulla base di dati clinici e studi retrospettivi. L’obiettivo è verificare che il modello in vitro sia in grado di riflettere ciò che avviene in vivo.
Successivamente, in una fase più avanzata che richiederà ulteriori finanziamenti, sarà possibile ampliare il sistema e utilizzarlo per produrre nuova conoscenza.
Per quanto riguarda lo stato attuale, abbiamo già condotto studi preliminari che ci hanno permesso di raccogliere dati e dimostrare la fattibilità dell’approccio. Siamo già in grado, su scala ridotta, di creare questi costrutti tridimensionali contenenti cellule del fluido amniotico. Durante il progetto lavoreremo per rendere il processo sempre più standardizzato, controllabile e scalabile — caratteristiche essenziali per un modello sperimentale affidabile.
Che cosa si intende esattamente per “piattaforma sperimentale”?
In questo contesto, si intende un sistema integrato che comprende diversi elementi: le cellule, un materiale di supporto (come un gel) in cui le cellule vengono inserite, e un insieme di condizioni sperimentali controllate che permettono di farle crescere e testarle in modo replicabile.
In pratica, si può immaginare una struttura composta da molti piccoli compartimenti — i cosiddetti “pozzetti” — all’interno dei quali vengono coltivati questi costrutti tridimensionali. In ciascun pozzetto si possono inserire cellule provenienti da pazienti diversi e testare differenti farmaci a concentrazioni variabili.
Scalando questo approccio, si possono arrivare a testare contemporaneamente molti pazienti, numerosi farmaci e diverse concentrazioni, generando centinaia o migliaia di condizioni sperimentali in parallelo.

Processo di 3D Bioprinting di costrutti fetali – Credits: Valerio Fausti
Entrando nella parte tecnica, che cosa significa stampare tessuti fetali con il 3D bioprinting? Come funziona?
Il 3D bioprinting è una tecnologia che basa su principi simili a quelli della stampa tradizionale o della stampa 3D: in particolare, alcune tecniche prevedono la deposizione di un materiale, strato dopo strato, fino a formare una struttura tridimensionale.
Nel caso del bioprinting, però, al posto di materiali plastici o inchiostri si utilizzano biomateriali — generalmente gel con proprietà biologiche adeguate — che contengono al loro interno cellule vive. In questo modo, si possono “stampare” veri e propri costrutti biologici tridimensionali, composti da una matrice di supporto e da cellule.
Perché le cellule derivate dal liquido amniotico sono particolarmente adatte per creare questi modelli?
Ci sono due motivi principali. Il primo è che queste cellule permettono di costruire modelli in vitro che riflettono direttamente le caratteristiche biologiche del feto.
Il secondo riguarda l’accessibilità: si tratta infatti di una fonte cellulare ottenibile senza procedure eccessivamente invasive e senza particolari criticità etiche. In molti casi, il liquido amniotico viene già prelevato nell’ambito di procedure cliniche come l’amniocentesi o altri interventi prenatali, ad esempio per finalità diagnostiche.
Da chi è composto il vostro gruppo di ricerca e con chi collaborate?
Il nostro è un gruppo fortemente multidisciplinare, proprio perché lavoriamo su tematiche molto diverse e trasversali. Al suo interno ci sono competenze che spaziano dai biomateriali al bioprinting, dalla biologia cellulare alla bioinformatica, fino all’ambito clinico: collaboriamo infatti con chirurghi pediatrici e ginecologi. Questa varietà riflette la complessità delle domande di ricerca che affrontiamo.
Sul piano scientifico, collaboriamo con alcuni centri di riferimento internazionali: l’Ospedale Bambino Gesù di Roma, l’ospedale e l’università di Leuven in Belgio e UCL a Londra. Si tratta di istituzioni molto attive nei campi della chirurgia fetale, della medicina rigenerativa e della ricerca prenatale e neonatale. Le collaborazioni con questi centri non si limitano a questo progetto, ma fanno parte di una rete di lavoro più ampia e consolidata.

Il gruppo del Prof Pellegata che svolge ricerca presso il LaBS-Laboratory of 3D Bioprinting and TIssue Engineering. Da sinistra a destra: Alessandro Mariani, Carlotta Casamassima, Alessandro Pellegata, Francesco Masala (collaboratore dal gruppo LaBS-uFluid), Giuseppe Guagliano – Credits: Valerio Fausti
Quale potrebbe essere l’impatto medico e sociale del progetto?
L’obiettivo principale è sviluppare uno strumento che oggi manca: un sistema affidabile per valutare gli effetti dei farmaci sul feto. Se questo strumento si dimostrerà valido, potrà essere utilizzato in futuro per testare nuovi farmaci. In questo senso, l’impatto immediato del progetto è metodologico: creare una base solida su cui costruire studi successivi.
In prospettiva, un modello di questo tipo potrebbe avere anche implicazioni più ampie. Si inserisce, ad esempio, nel contesto della medicina personalizzata, un approccio sempre più centrale nella ricerca biomedica, soprattutto in ambito oncologico. È ormai chiaro che pazienti diversi possono rispondere in modo molto diverso alle stesse terapie, in base a fattori genetici, ambientali e individuali.
Quali sono le principali sfide che state affrontando?
Dal punto di vista scientifico, la difficoltà principale riguarda la costruzione di modelli in vitro che siano davvero rappresentativi della realtà biologica. Quando si sviluppa un modello, infatti, si introducono inevitabilmente molte semplificazioni rispetto alla complessità di un organismo vivente. La sfida sta proprio nel capire quali semplificazioni siano accettabili e quali invece rischino di compromettere l’affidabilità del modello. Arrivare a un sistema che riesca a riprodurre in modo convincente ciò che avviene nell’essere umano è, senza dubbio, l’ostacolo più grande.
Che cosa ti ha colpito di più, dal punto di vista scientifico e umano, lavorando su questo progetto?
Uno degli aspetti più rilevanti, anche sul piano personale, riguarda il modo in cui viene vissuta la gravidanza. C’è ancora, almeno in parte, una visione culturale secondo cui la gravidanza viene trattata quasi come una condizione patologica, mentre in realtà è uno stato fisiologico. Oggi, fortunatamente, questa visione sta cambiando: si riconosce sempre di più che durante la gravidanza sia importante mantenere, per quanto possibile, uno stile di vita attivo.
In questo senso, uno degli aspetti che mi sta più a cuore è che, in prospettiva, progetti come questo possano contribuire a migliorare la qualità della vita delle donne in gravidanza. L’obiettivo è evitare che la gravidanza venga vissuta come un periodo di rinuncia — che si tratti di farmaci utili per il benessere quotidiano o, nei casi più complessi, di terapie fondamentali per la salute della madre.
In generale, l’idea è contribuire a una visione della gravidanza sempre più vicina alla sua natura fisiologica.









